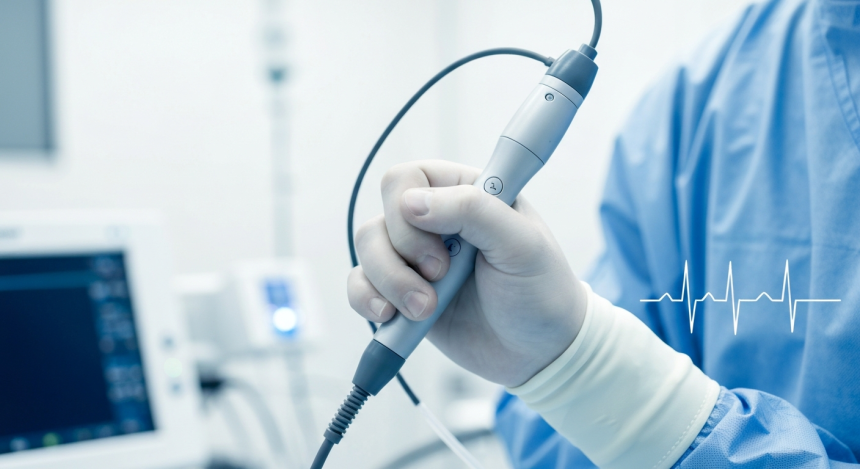
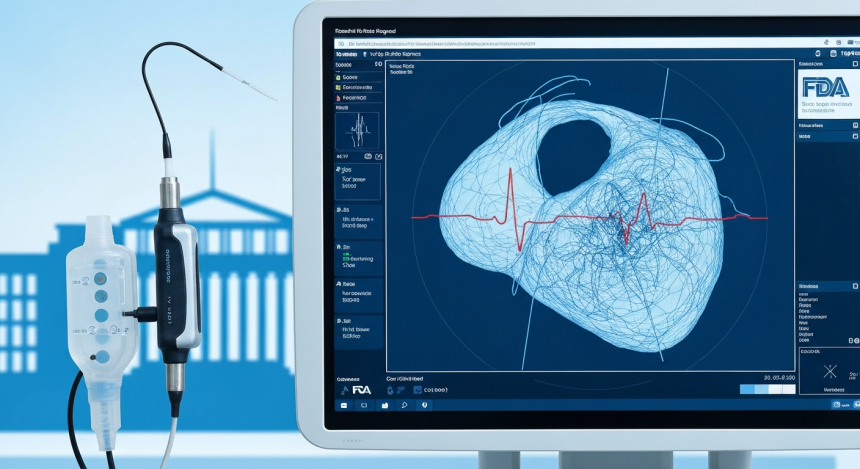
애지오 메디컬 홀딩스($ADGM)이 심실빈맥 치료용 냉동 절제 시스템 ‘vCLAS’의 미국 허가 신청에 활용할 핵심 임상 결과를 공개했다. 회사는 FULCRUM-VT 임상 6개월 추적 결과에서 안전성과 유효성 평가변수를 충족했다고 밝혔으며, 해당 내용은 미국심장리듬학회 2026 학술대회에서 발표됐다.
이번 시험에서 시술 직후 목표 심실빈맥이 더 이상 유도되지 않은 비율은 98%였다. 6개월 기준 삽입형 제세동기(ICD) 충격이 없었던 환자 비율은 84%, 모든 심실빈맥 재발이 없었던 비율은 59%로 집계됐다. 회사 측은 주요 이상반응 발생률이 2.4%에 그쳐 전반적으로 ‘양호한’ 안전성 프로필을 확인했다고 설명했다.
허혈성·비허혈성 심근병증서 유사 성과
FULCRUM-VT는 미국과 캐나다 20개 기관에서 진행된 전향적, 다기관, 공개, 단일군 IDE 임상으로, 약물 난치성 심실빈맥 환자 209명이 등록됐다. 환자군에는 허혈성 심근병증(ICM)과 비허혈성 심근병증(NICM)이 모두 포함됐다.
특히 시장의 관심은 서로 다른 기저질환군에서 비슷한 결과가 나왔다는 점에 쏠린다. 6개월 기준 기기 개입 없이 유지된 비율은 허혈성 심근병증 환자 61%, 비허혈성 심근병증 환자 63%였다. ICD 충격이 없었던 비율도 각각 84%, 85%로 거의 차이가 없었다. 회사는 현재 승인된 기술로는 치료가 까다로운 비허혈성 심근병증 환자에서도 심내막 접근만으로 비슷한 효과를 냈다는 점을 강조했다.
시술 효율성과 약물 감소 효과도 주목
평균 절제 시간은 환자당 54분, 평균 병변 수는 11.5개였다. 또 시술 후 6개월 동안 ICD 충격을 경험한 환자 수는 시술 전 같은 기간과 비교해 80% 넘게 감소했다. 아미오다론 복용 환자 가운데 72%는 약을 중단하거나 용량을 줄였다. VT 관련 30일 내 재입원율은 1.9%로 낮게 나타났다.
다만 안전성 수치에는 절차 전후 사망 사례도 포함됐다. 회사에 따르면 주요 이상반응에는 시술 전후 사망 4건, 즉 1.9%가 반영됐고, 이 가운데 2건은 독립적 임상사건위원회가 시험 기기와 ‘관련 가능성 있음’으로 판단했다. 안전성과 재발 관련 데이터는 모두 독립 위원회가 심사했다.
FDA 허가 심사 기대감
애지오 메디컬은 이번 데이터를 바탕으로 미국 식품의약국(FDA)에 vCLAS의 시판 전 승인(PMA)을 신청할 계획이다. 현재 이 시스템은 유럽 등 일부 지역에서는 상업 판매 중이지만, 미국에서는 임상용으로만 사용이 제한돼 있다.
의료진 평가는 대체로 긍정적이다. 아툴 버마 박사는 허혈성과 비허혈성 구조적 심질환 환자를 함께 포함한 대규모 중추 임상에서 ‘임상적으로 의미 있는’ 결과가 나왔다고 평가했다. 매슈 하키미 메디컬 디렉터도 기존 고주파 절제와 새롭게 등장한 펄스장 절제 방식과 비교해 경쟁력 있는 결과라고 설명했다.
이번 결과는 심실빈맥 절제술 시장에서 ‘심내막 단독 접근’의 가능성을 넓혔다는 점에서 의미가 있다. 다만 최종 판단은 FDA 심사와 장기 추적 결과에서 가려질 전망이다. 회사가 제시한 수치가 실제 표준 치료 변화로 이어질지는 추가 검증이 필요하다.
TP AI 유의사항 TokenPost.ai 기반 언어 모델을 사용하여 기사를 요약했습니다. 본문의 주요 내용이 제외되거나 사실과 다를 수 있습니다.
















 0
0








![[토큰명언]](https://f1.tokenpost.kr/2026/04/2m0cqrioyh_th_860x0.webp)



![[자정 뉴스브리핑] 블랙록 IBIT 비트코인 옵션 OI, 데리빗 첫 추월 外](https://f1.tokenpost.kr/2026/04/9n0t7yhtxb_th_860x0.webp)
![[자정 시세브리핑] 암호화폐 시장 혼조세… 비트코인 78,117달러, 이더리움 2,347달러](https://f1.tokenpost.kr/2026/04/musvnfjwdn_th_860x0.webp)
![[에너지분석] 이란 전쟁이 바꾼 중국의 선택… 미국산 에탄 수입 사상 최대](https://f1.tokenpost.kr/2026/03/7s8m816fu8_th_860x0.jpg)
![[토큰분석] 미국 세금 환급액 2,417억 달러… 비트코인 리테일 수요 '깜짝 촉매' 되나](https://f1.tokenpost.kr/2026/04/f2xcrxls4p_th_860x0.jpg)
![[로보분석] 골드만삭스](https://f1.tokenpost.kr/2026/03/0scauhmod4_th_860x0.webp)






![[Episode 12] IXO™2024 참여하고, 2억원 상당 에어드랍 받자!](https://f1.tokenpost.kr/2024/03/bk2tc5rpf6_th_860x0.png)
![[Episode 11] 코인이지(CoinEasy) 에어드랍](https://f1.tokenpost.kr/2024/02/g0nu4cmps6_th_860x0.png)
![[Episode 8] Alaya 커뮤니티 입장하고, $AGT 받자!](https://f1.tokenpost.kr/2023/10/0evqvn0brd_th_860x0.png)
![[Episode 6] 아트테크 하고, 에어드랍 받자!](https://f1.tokenpost.kr/2023/08/3b7hm5n6wf_th_860x0.webp)
![[토큰포스트] 기사 퀴즈 584회차](https://f1.tokenpost.kr/2026/04/1pi2l2c6ct_th_860x0.png)
![[토큰포스트] 기사 퀴즈 583회차](https://f1.tokenpost.kr/2026/04/43zq77fvbs_th_860x0.webp)
![[토큰포스트] 기사 퀴즈 581회차](https://f1.tokenpost.kr/2026/04/9epgx2rg9j_th_860x0.webp)
![[토큰포스트] 기사 퀴즈 580회차](https://f1.tokenpost.kr/2026/04/1d4yk2lv4f_th_860x0.webp)



![[특징주] 호텔신라, 1분기 흑자전환·이부진 200억 자사주 매입에 5%대 강세](https://f1.tokenpost.kr/2026/04/8bmnoq012r_th_860x0.jpg)

![[특징주] 현대백화점, 지배구조 개편·주주환원 기대에 강세](https://f1.tokenpost.kr/2026/04/cieuuocv3m_th_860x0.jpg)
![[특징주] SK하이닉스, 장중 신고가 경신…HBM 경쟁력에 130만원 기대](https://f1.tokenpost.kr/2026/04/iuggepuuju_th_860x0.jpg)